Kovalent Bağlar ders notları, konu anlatımı pdf, konu özeti, konu anlatımı pdf, konuları, test pdf, çalışma kağıdı, ders kitabı cevapları, çalışma kitabı cevapları ve yazılı soruları.
Kovalent Bağlar
Kovalent Bağlar Ders Notu Konu Özeti İndir
Kovalent Bağlar
Elektronegatiflikleri birbirine yakın veya aynı olan atomların elektronlarını ortaklaşa kullanmaları sonucunda oluşan bağa kovalent bağ denir. H2, F2, Cl2, O2, P4 , S8 kovalent bağlı moleküllerdir.
Lewis kuralına göre;

Cl ile Cl birer elektronlarını ortaklaşa kullanarak kovalent bağ oluşturur. Bu elektron çifti bağ olarak çizgi şeklinde gösterilir. Cl-Cl
Aynı iki atom arasında bir elektron çiftinden daha fazla elektron ortaklaşa kullanılabilir. Buna çoklu kovalent bağ ismi verilir. Çift bağda, iki atom arasında iki elektron çifti, üç bağda ise üç elektron çifti bulunur.
Kovalent Bağlı Moleküllerden Oluşan Maddelerin Özellikleri
Kovalent bağlı moleküllerden oluşan maddeler, iyonik ve metalik bağlı maddelere göre daha düşük kaynama ve erime noktasına ve ayrıca daha düşük erime ve buharlaşma ısılarına sahiptirler. Çünkü bir iyonik bileşiği eritirken çok kuvvetli olan iyonik bağları kırmak için yüksek sıcaklığa ısıtmak gereklidir. Halbuki moleküllerden oluşan bir katı maddeyi eritmek için iyonik bağa göre çok daha zayıf olan moleküller arası çekim kuvvetlerini yenmek, gerekeceğinden daha düşük bir sıcaklığa ısıtmak yeterli olacaktır. Düşük yoğunlukludurlar, gaz, sıvı ve katı haldedirler. Katı halde iken kırılgan ve zayıf yumuşak veya mumsu bir yapıları vardır. Elektrik ve ısıyı çok az iletirler. Genellikle organik çözücülerle çözünebilirler.
Polar kovalent Bağlar :
Elektronegatiflikleri birbirinden farklı iki atomun oluşturduğu kovalent bağlarda ortak kullanılan elektron çifti eşit olarak paylaşılmaz. Daha elektronegatif olan atom tarafından bu elektron çifti daha fazla çekilir ve böylece polar kovalent bağ oluşur.
Bazı atomlar arasındaki elektronegatiflik sırası aşağıda verilmiştir.
F > O > N > Cl > Br > C > I > H
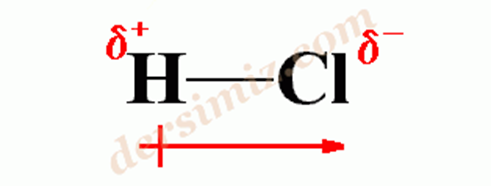
Cl (klor) atomunun elektronegatifliği H (hidrojen) atomundan çok fazla olduğu için ortak elektronlar klor atomu tarafından daha çok çekilir ve hidrojen kısmi pozitif yükle yüklenirken, klor kısmi negatif yükle yüklenir. Böylelikle dipol moment oluşur.Dipol momenti olan moleküller polardır.
Koordine Kovalent Bağlar :
Bağ yapmak için elektronlar tek atom tarafından veriliyorsa, bu tür kovalent bağlara koordine kovalent bağ denir.
N (azot) atomu üç bağ yapabilir. N atomu üzerinde bulunan ortaklanmamış elektron çifti hidrojenle dördüncü bağ yapımında kullanılır. Böylece bu bağın oluşumunda elektronlar azot tarafından sağlanmış olur.

İşinize Yarayabilir
Kimya Ders Notları, Çalışma Notları, Konu Özetleri Ana Sayfa
Ders Kitabı Cevapları
Tüm Dersler Test Pdf İndir ve Online Test Çöz
Yazılı Soruları Tüm Sınıflar
